Scientific Kalender April 2019
Wie kann der automatisierte direkte Nachweis von mit Malaria infizierten roten Blutzellen (RBZ) den weltweiten Kampf gegen Malaria unterstützen?
Malaria kann grundsätzlich ausgeschlossen werden, wenn ein hochsensitiver, diagnostischer Schnelltest (rapid diagnostic test, RDT) für Malaria negativ ist.
Wenn in einem peripheren Blutausstrich eines fiebrigen Patienten bei der lichtmikroskopischen Untersuchung keine mit Malaria infizierten RBZ gefunden werden, kann davon ausgegangen werden, dass das Fieber nicht durch Malaria verursacht wird.
Die automatisierte XN-31-Technologie ermöglicht eine schnelle, sorgfältige und präzise Quantifizierung von mit Malaria infizierten RBZ. Dies erleichtert die Überwachung der abnehmenden Parasitenlast und somit auch der therapeutischen Wirksamkeit nach Einleitung einer Behandlung mit Malaria-Medikamenten.
Die RDTs für Malaria können effektiv für die Überwachung des Ansprechens auf Malaria-Medikamente verwendet werden.
Herzlichen Glückwunsch!
Das ist die richtige Antwort.
Das ist leider nicht komplett richtig.
Bitte versuchen sie es erneut.
Das ist leider nicht die richtige Antwort.
Bitte versuchen sie es erneut.
Hinweis
Bitte wählen sie mindestens eine Antwort aus.
Wissenschaftliche Hintergrundinformationen
Malaria ist auch weiterhin weltweit eine der größten Gefahren für die öffentliche Gesundheit: in den 91 Ländern mit einem Infektionsrisiko leben 3,2 Milliarden Menschen [1]. Dem World Malaria Report der WHO aus dem Jahr 2017 ist zu entnehmen, dass nach einem bemerkenswerten Zeitraum mit erfolgreicher globaler Malaria-Kontrolle die Fallzahlen wieder einmal steigen und der Fortschritt ins Stocken geraten ist. Es müssen erhebliche Anstrengungen unternommen werden, um diesen Trend umzukehren. Jeder verhinderte Malaria-Fall und jeder abgewendete Todesfall sind ein Beitrag zur globalen Kampagne zur Ausrottung von Malaria.
Ein kritischer Aspekt im Rahmen der Bemühungen rund um die Malaria-Kontrolle ist die frühzeitige und richtige Diagnose. Die WHO empfiehlt für alle Malaria-Verdachtsfälle die Durchführung eines Parasitentests (entweder mikroskopisch oder in Form eines RDT). Diese Maßnahme dient der Vermeidung mutmaßlicher Therapien auf alleiniger Basis eines klinischen Verdachts und der Minimierung einer unnötigen Exposition gegenüber Malaria-Medikamenten.
Die mikroskopische Untersuchung eines peripheren Blutausstrichs ermöglicht die direkte Sichtbarmachung von Parasiten in infizierten RBZ und ist der aktuelle diagnostische Goldstandard. Allerdings ist diese Art der Untersuchung in hohem Maße subjektiv, da die Nachweisgrenze deutlich von dem Kompetenzniveau und der Sorgfalt der untersuchenden Person abhängig ist. Infolgedessen werden in der Routinepraxis regelmäßig submikroskopische Malariainfektionen mit einer geringen Erregeranzahl übersehen; hiervon sind insbesondere Schwangere unverhältnismäßig betroffen. Diese Situation wird noch durch den Umstand erschwert, dass die Nichtdiagnose einer Malaria-Infektion bei bestehender Schwangerschaft sowohl die werdende Mutter als auch das Ungeborene einem hohen Mortalitätsrisiko aussetzt.
Auf der anderen Seite sind immunchromatografische RDTs sehr anwenderfreundlich und daher als Stand-alone- oder Zusatztest zur Mikroskopie weit verbreitet. RDTs beruhen auf dem indirekten Nachweis von Malaria auf Basis vorliegender Malaria-Antigene oder -Proteine [2]. Allerdings verfügen RDTs auch über verschiedene Nachteile: (1) sie können nicht zwischen einer akuten und einer kürzlich behandelten Infektion unterscheiden, (2) sie sind nicht quantitativ und können damit nicht zur Überwachung der Wirksamkeit einer Behandlung herangezogen werden, (3) nicht alle dieser Tests weisen Plasmodium-Spezies nach und (4) sie weisen weder eine Spezifität (Kreuzreaktivität gegenüber anderen Antigenen wie dem Rheumafaktor) noch eine Sensitivität (im Vergleich zu einer Fachperson, die die mikroskopische Untersuchung durchführt) auf. In Erwartung eines größeren Anteils an Infektionen mit einer geringen Erregeranzahl bei verbesserter Malaria-Kontrolle und angesichts Ländern, die Malaria aktiv ausrotten, wurden hochsensitive RDTs für das histidinreiche Protein-2 (HRP2) von P. falciparum als Ziel-Antigen entwickelt. Allerdings wird der erwartete Nutzen einer verbesserten Sensitivität durch die Entdeckung von Mutationen im HRP2-Gen von P. falciparum, dem häufigsten und tödlichsten der Malaria-Parasiten, relativiert. Folglich wird jeder HRP2-basierte RDT mit steigender Verbreitung dieser Mutationen weniger effektiv.
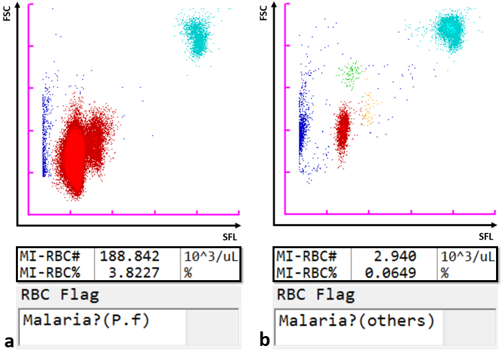
Unter Verwendung seines Halbleiterlasers mit einem 405-nm-Strahl, der den Nachweis kleinerer Partikel ermöglicht, kann das Hämatologie-Analysesystem XN-31 von Sysmex zusätzlich zu den Parametern des großen Blutbilds auf Basis der Fluoreszenz-Durchflusszytometrie auch mit Malaria infizierte RBZ (MI-RBZ) detektieren und zählen. Die RBZ werden teilweise permeabilisiert und können so Fluoreszenzmarker aufnehmen, die in infizierten Zellen die Nukleinsäure von Malaria-Parasiten anfärben. Die Intensität des Seitwärts-Fluoreszenzlichts (SFL) und das Signal des Vorwärts-Streulichts (FSC) werden grafisch gegeneinander abgetragen, um ein so genanntes Malaria(M)-Scattergramm zu erhalten. Während des asexuellen Lebenszyklus wachsen eine infizierte RBZ und deren anfärbbarer Nukleinsäuregehalt bei der sequenziellen Ausbildung der Ringformen von Trophozoiten und Schizonten. Gleichermaßen sind Gametozyten, die sich nach einem entwicklungsbedingten Auslöser hin zur sexuellen Reproduktion bilden, eindeutig identifizierbar. Demnach kategorisiert das XN-31-Analysesystem eine Malaria-Infektion in einer Probe anhand der Stadien des Lebenszyklus basierend auf dem SFL (Menge an Nukleinsäure) und dem FSC (Größe der MI-RBZ). Unterschiedliche Plasmodium-Spezies weisen verschiedene Scattergramm-Muster auf; diese werden von der Software des Analysesystems zur Identifizierung der vermeintlichen Spezies (P. falciparum oder eine andere Spezies) verwendet.
Die untere Nachweisgrenze des Analysesystems liegt bei 20 Parasiten/μl. Dieser Wert liegt deutlich unter der Nachweisgrenze regulärer RDTs und routinemäßiger mikroskopischer Untersuchungen von peripheren Blutausstrichen (≥ 100 Parasiten/μl [3] ).
Das XN-31-Analysesystem ist eine ideale Modalität für die genaue Erkennung und schnelle, automatisierte Auszählung einer Malaria-Parasitämie, und zwar unabhängig von der Kompetenz des Bedieners oder der vorliegenden Spezies. Das System weist den tatsächlichen Parasiten und nicht Nebenprodukte wie Antigene, Hämozoin oder von weißen Blutzellen phagozytierte Parasiten nach. Aus diesem Grund ist dieses System im Vergleich zu RDTs und anderen indirekten, automatisierten Methoden für den Nachweis von Malaria die geeignetere Wahl [4]. Darüber hinaus verfügt dieses Analysesystem mit der zeitgleichen Erstellung eines großen Blutbilds, welches wertvolle Daten für die klinische Korrelation liefert, um ein Alleinstellungsmerkmal.
Scattergramme
Literatur
1. WHO. World malaria report 2018. Genf: Weltgesundheitsorganisation; 2018. http://www.who.int/malaria/publications/world-malaria-report-2018/en/.
2. Chotivanich K, Silamut K, Day N. Laboratory diagnosis of malaria infection ‒ A short review of methods. N Z J Med Lab Sci. 2007; 61:4-7.
3. WHO. Policy brief on malaria diagnostics in low transmission settings. Genf: Weltgesundheitsorganisation; 2014. https://www.who.int/malaria/publications/atoz/malaria-diagnosis-low-transmission-settings-sep2014.pdf?ua=1
4. Pillay E, Khodaiji S, Bezuidenhout BC, Litshie M, Coetzer TL. Evaluation of automated malaria diagnosis using the Sysmex XN-30 analyser in a clinical setting. Malar J. 2019; 22. Januar; 18(1):15. doi: 10.1186/s12936-019-2655-8.