MammaTyper®
Umfassende molekulare Subtypisierung von Brustkrebs
- Präzise Bestimmung von HER2, ER, PR und Ki-67 in einem einzigen Assay
- Eindeutige Subtypisierung von Brustkrebs für sichere Behandlungsentscheidungen
- Einfach zu handhaben, quantitativ und standardisiert
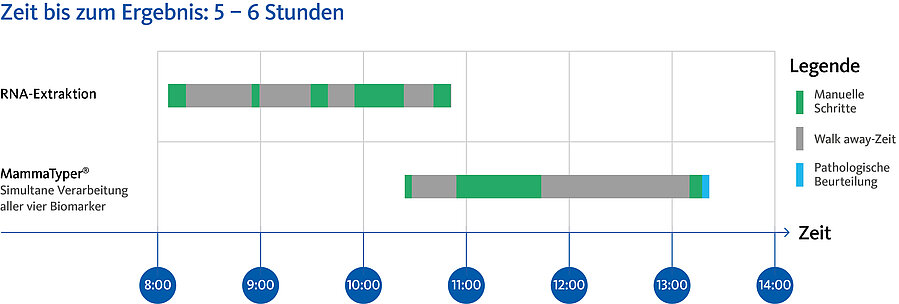
- Schnelle Durchlaufzeit mit Ergebnissen innerhalb desselben Tages
- CE-gekennzeichneter IVD RT-qPCR-Assay, validiert für die gängigsten Thermocycler
- Auch erhältlich: RNXtract® RNA Extraktions-Kit für FFPE-fixiertes Gewebe
MammaTyper® quantifiziert präzise die Expression von HER2, ER, PR und Ki-67 mRNA
MammaTyper® ist ein molekulardiagnostischer Test zur quantitativen Bestimmung der vier wichtigsten Biomarker, die für die Subtypisierung von Brustkrebs verwendet werden. Diese Biomarker sind der humane epidermale Wachstumsfaktor-Rezeptor 2 (HER2), der Östrogenrezeptor (ER), der Progesteronrezeptor (PR) und der Proliferationsmarker Ki-67.
Die Kombination der Biomarker-Expression ermöglicht die Bewertung der verschiedenen Brustkrebs-Subtypen als wichtigen Parameter für Behandlungsentscheidungen.
Definition von Brustkrebs-Subtypen
(St. Gallen 2013)
| Brustkrebs-Subtypen | ER | PR | HER2 | Ki-67 |
| Luminal A-like | Pos | Pos | Neg | Neg |
| Luminal B-like (HER2 negative) | Pos | Pos/Neg* | Neg | Pos/Neg* |
| Luminal B-like (HER2 positive) | Pos | Pos/Neg | Pos | Pos/Neg |
| HER2 positive (non-luminal) | Neg | Neg | Pos | Pos/Neg |
| Triple negative (ductal) | Neg | Neg | Neg | Pos/Neg |
*mit Ausnahme der Kombination PR pos und Ki-67 neg = Luminal A-like
MammaTyper® wurde entwickelt, um den Bedarf an einer standardisierten, quantitativen und schnellen molekularen Subtypisierung zu decken, die sichere Behandlungsentscheidungen ermöglicht.
Mit RNXtract bieten wir ergänzend ein optimiertes RNA Extraktions-Kit für FFPE-fixiertes Gewebe an. RNXtract ist ebenfalls CE-IVD gelabelt. Die RNA-Extraktion erfolgt mittels Magnetic Beads. Ein Kit ist ausreichend für 48 Proben.
MammaTyper® ist ein einfach durchzuführender Test für jedes Pathologielabor, der innerhalb von 6 Stunden präzise Ergebnisse liefert.
| 1 | Probenvorbereitung | 10 μm FFPE-Gewebeschnitt (Tumorzellgehalt > 20 %) |
| 2 | RNA-Extraktion | Die Verwendung eines RNA-FFPE-Probenextraktionskits gemäß der Gebrauchsanweisung oder eines validierten kommerziellen RNA-Extraktionssystems wird empfohlen. |
| 3 | MammaTyper® Test-Setup | Vorbereitung der Mastermixe und Verteilung auf 96-Well-Platten, Analyse von bis zu 8 Patientenproben pro Lauf |
| 4 | RT-qPCR-Analyse | Validiert mit den folgenden qPCR-Systemen:
|
| 5 | Datenverarbeitung und Berichterstellung | Übersichtliche und bedienerfreundliche MammaTyper® Report Generator Software:
|
MammaTyper® ist als Marke in verschiedenen Ländern exklusiv an Cerca Biotech www.cercabiotech.com lizenziert.
| Bezeichnung | MammaTyper® IVD Test Kit (10 Reaktionen) |
| Probentyp | 10 μm FFPE-Gewebeschnitt (Tumorzellgehalt > 20 %) |
| Probenkapazität | Bis zu 8 Patientenproben pro Kit |
| Qualitätskontrolle | 2 externe Kontrollmaterialien (positiv + negativ) |
| Kompatible Plattformen | LightCycler® 480 Instrument II (Roche) Cobas z® 480 Analyzer (Roche) Versant® kPCR AD module (Siemens) Applied Biosystems® 7500 Fast (Dx) RT PCR (ThermoFisher Scientific) CFX96TM RT PCR Detection System-IVD (BIO-RAD®) MX3000P (Agilent®) Agilent® AriaDx Real-Time PCR System (Agilent®) SLAN®-96P Real-Time PCR System (Sanure Biotech) |
| Konkordanz | Konkordanz zwischen MammaTyper® und IHC/CISH-basierten Biomarker-Bewertungen: HER2 91,8 %, ER 91,8 %, PR 82,5 %, Ki-67 75,0 % 1 |
| Reproduzierbarkeit | Die Reproduzierbarkeit der binären Einzelmarkerergebnisse (positiv/negativ) sowie die Übereinstimmung der molekularen Subtypen war in einer Konkordanzstudie an 10 Zentren nahezu perfekt (Kappa-Werte: 0,90 - 1,00) 2 |
| Reklassifizierung | MammaTyper® kann eine präzisere Bewertung des endokrinen Ansprechens ermöglichen, die Ki-67-Standardisierung verbessern und zur Klärung von nicht eindeutigen HER2-IHC/FISH-Fällen beitragen, was zu einer möglichen Neubewertung der molekularen Subtypen führt 3 |
| Artikelnummer | CC01010 |
Referenzen
- Wirtz RM et al., Breast Cancer Res Treat 2016; 157(3), 437446
- Varga Z et al., Breast Cancer Res 2017; 19(55), 1-13
- Caselli E et al., PLOS ONE 2021; 16(9), 1-18
- Shaaban A et al., Eur J Cancer 2022; 175(1), 87-88
Sysmex Deutschland GmbH
Bornbarch 1
22848 Norderstedt
+49 (40) 534 10 2-0
+ 49 (40) 523 23 02
Produkt-Dokumente
Regulatorische Dokumente
Auf regulatorische Dokumente, wie Bedienungsanleitungen, können Sie mit Ihrem Account in unserem Kundenportal zugreifen:
Zu My Sysmex