Plasma-SeqSensei™ Breast Cancer IVD Kit
Plasma-SeqSensei™ Breast Cancer IVD Kit
- Bildet die Heterogenität metastasierter Erkrankung ab
- Validierte, IVD-zertifizierte Liquid Biopsy (Flüssigbiopsie)
- Hochsensitiv von 0,06 % und höhere mutierte Allelfraktion (MAF) bei einem DNA-Input von 10.000 GE.
- Quantitativer Nachweis von 6 oder mehr mutierten Molekülen mit 95%iger Sicherheit
- Schnelle Durchlaufzeit von nur 2 Tagen
- Bequeme Datenanalyse und Berichterstellung mit IVD-zertifizierter Software
- Minimalinvasive patientenfreundliche Blutabnahme
- Therapieentscheidung und Krebsbehandlung unterstützen
Plasma-SeqSensei™ Assays ermöglichen einen hochsensitiven und quantitativen Nachweis von Mutationen in zirkulierender Tumor-DNA (ctDNA) aus dem Blutplasma von Patientinnen mit Mammakarzinom basierend auf Next Generation Sequencing (NGS) Technologie.
Durch den kurzen und standardisierten Arbeitsablauf von Plasma-SeqSensei werden Ergebnisse innerhalb von zwei Tagen geliefert, einschließlich der Erstellung von leicht lesbaren Berichten mit der Plasma-SeqSensei™ IVD-Software. Das Kit deckt Mutationen in den krebsrelevanten Genen AKT1, ERBB2, ESR1, KRAS, PIK3CA und TP53 ab, um etablierte und neu entstehende prädiktive Marker, Resistenzmutationen sowie häufig auftretende genetische Veränderungen beim Mammakarzinom zu detektieren.
Das Plasma-SeqSensei Breast Cancer IVD Kit unterstützt Kliniker bei:
- Therapieentscheidung und Krebsbehandlung
- Nachweis einer minimalen Resterkrankung (MRD)
- Erkennung von Krankheitsprogression, Resistenzentwicklung gegen die Therapie und klonale Entwicklung
- Früher Erkennung und Überwachung von Rezidivbildung
- Monitoring des (neo-) adjuvanten Therapieansprechens
Plasma-SeqSensei Technologie
Zuverlässige Detektion von Mutationen
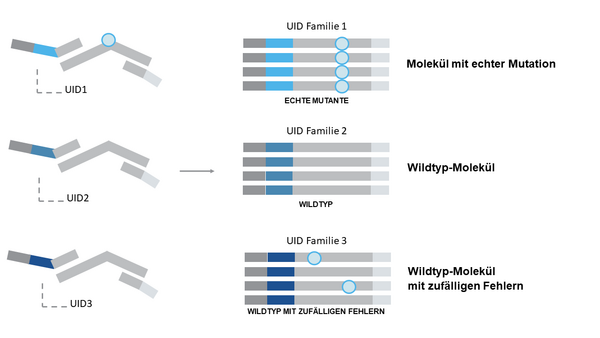
Um die Sensitivität zu erhöhen und die mit der Sequenzierung verbundenen Fehlerquoten zu verringern, wird imPlasma-SeqSensei-Arbeitsablauf zur Erstellung der Bibliothek die SafeSEQ-Technologie1 eingesetzt. Diese Technologie weist jedem DNA-Molekül einen molekularen eindeutigen Unique Identifier (UID) zu. UIDs helfen echte Mutationen in Proben zu detektieren und von Fehlern der Polymerase oder der Sequenzierung zu unterscheiden. Plasma-SeqSensei erkennt mit 95%iger Sicherheit 0,06 % und höhere Tumorfaktion / mutierte Allefraktion (MAF) in einem Hintergrund von 10.000 Wildtyp-Kopien.
Mehr als MAF - absolute Quantifizierung von Mutationen
Die Plasma-SeqSensei-Technologie verwendet ein internes Referenzmolekül, genannt Quantispike, das eine robuste Quantifizierung tumorspezifischer Sequenzen über einen breiten dynamischen Bereich bis zu einer unteren Nachweisgrenze (LOD) von 6 Mutationen ermöglicht. Dies ermöglicht eine absolute Quantifizierung der im untersuchten Blutvolumen nachgewiesenen Mutationen und damit einen aussagekräftigen Vergleich der Veränderungen der ctDNA-Konzentrationen im Lauf der Therapie.
Plasma-SeqSensei™ IVD Software
Die Plasma-SeqSensei IVD-Software bietet die Möglichkeit, Sequenzierungsläufe mühelos zu planen und zu analysieren sowie Daten einfach zu erfassen. Es ist die erste IVD-zertifizierte Software, die auf einem PC oder Laptop läuft - eine Workstation oder Serverstruktur ist nicht erforderlich. Die Oberfläche ist in drei Funktionsmodule unterteilt: Laufplanung, Datenanalyse und Berichterstellung. Zu den automatisch erstellten Berichten gehören Probenmetriken und Mutationsstatus, die sowohl die MAFs als auch die absolute Anzahl der im Probenvolumen nachgewiesenen mutierten Moleküle auflisten, sowie Metriken zur Sequenzierungsqualität.
Referenzen
- Kinde, I., Wu, J., Papadopoulos, N., Kinzler, K. W., & Vogelstein, B. (2011). Detection and quantification of rare mutations with massively parallel sequencing. Proceedings of the National Academy of Sciences of the United States of America, 108(23), 9530–9535. https://doi.org/10.1073/pnas.1105422108
| Plasma-SeqSenseiTM Breast Cancer IVD Kit | |
| Typ | Vollblut und Blutplasma |
| Kapazität | 2–16 Proben pro Kit und bis zu 32 Proben mit dem PSS Extension IVD Kit |
| QC Funktion | Positivkontrolle und Negativkontrolle (NTC) bei jedem Durchlauf |
| kompatible Sequenzierer | Illumina NextSeq 500/550™ |
| Notwendiger DNA Input | 4,3–86 ng/116 µl |
| Anzahl der Amplikons | 28 |
| Sensitivität | 0,06 % Allelfraktion mit 95%iger Sicherheit bei 10.000 Wildtyp-Kopien |
| Cut-off | 6 mutierte Moleküle |
| Artikelnummer | ZR150544 |
Zielgene
| Gene ID# | Transkript ID# | Start der kodierenden Sequenz | Ende der kodierenden Sequenz | Die häufigsten detektierten Mutationen |
| AKT1 | ENST00000554581 | 47 | 69 | E17K |
| ERBB2 | ENST00000269571 | 907 | 947 | S310F |
| ERBB2 | ENST00000269571 | 2,308 | 2,360 | L755S, D769Y |
| ERBB2 | ENST00000269571 | 2,258 | 2,307 | V777L |
| ESR1 | ENST00000440973 | 1,108 | 1,143 | E380Q |
| ESR1 | ENST00000440973 | 1,378 | 1,420 | S463P |
| ESR1 | ENST00000440973 | 1,583 | 1,614 | D538G, Y537S/C/N |
| KRAS | ENST00000256078 | 8 | 43 | G12D/V/C/R/A/S, G13D |
| PIK3CA | ENST00000263967 | 254 | 278 | R88Q |
| PIK3CA | ENST00000263967 | 329 | 352 | K111E |
| PIK3CA | ENST00000263967 | 353 | 367 | G118D |
| PIK3CA | ENST00000263967 | 1,033 | 1,058 | E345K |
| PIK3CA | ENST00000263967 | 1,085 | 1,115 | P366R |
| PIK3CA | ENST00000263967 | 1,252 | 1,264 | C420R |
| PIK3CA | ENST00000263967 | 1,348 | 1,387 | E453K |
| PIK3CA | ENST00000263967 | 1,611 | 1,659 | E545K/A, E542K |
| PIK3CA | ENST00000263967 | 2,138 | 2,184 | E726K |
| PIK3CA | ENST00000263967 | 3,118 | 3,169 | H1047R/L |
| TP53 | ENST00000269305 | 144 | 232 | W53* |
| TP53 | ENST00000269305 | 293 | 375 | R110P |
| TP53 | ENST00000269305 | 376 | 423 | C141Y, C135Y |
| TP53 | ENST00000269305 | 451 | 537 | R175H, H179R |
| TP53 | ENST00000269305 | 574 | 659 | R213*, Y220C, R196* |
| TP53 | ENST00000269305 | 695 | 782 | R248Q/W, G245S |
| TP53 | ENST00000269305 | 783 | 856 | R273H/C, R282W |
| TP53 | ENST00000269305 | 888 | 919 | R306* |
| TP53 | ENST00000269305 | 920 | 993 | Q331* |
| TP53 | ENST00000269305 | 994 | 1,080 | R342* |
Sysmex Deutschland GmbH
Deelböge 19 D
22297 Hamburg
+49 (40) 534 10 2-0
+ 49 (40) 523 23 02
Produkt-Dokumente
Regulatorische Dokumente
Auf regulatorische Dokumente, wie Bedienungsanleitungen, können Sie mit Ihrem Account in unserem Kundenportal zugreifen:
Zu My Sysmex