Wenn aus selten immer öfter wird
XTRA-ARTIKEL AUSGABE 1/2022
Seltene RBC-Erkrankungen kommen durch die Globalisierung auch in Nordeuropa immer häufiger vor, weshalb Klinikerinnen und Kliniker ihre Erfahrungen weiter ausbauen müssen
Text: Ramona El-Fatmi

Nelson* (Name geändert), ein junger Student aus dem Senegal, war erst wenige Wochen in Deutschland und sprach nur gebrochen Deutsch, als er während des Spielens bei einem Fußballturnier unter heftigen Bauchschmerzen zusammenbrach. Wenig später verlor er das Bewusstsein. Nach zügiger Notaufnahme stellte der behandelnde Arzt mithilfe der explorativen Laparoskopie multiple Gefäßverschlüsse fest. Unter anderem waren die Milzvene und die Pfortader vollständig thrombosiert. Eine Lungenarterienembolie führte zum akuten Cor pulmonale und schließlich zum Rechtsherzversagen. Der Patient verstarb auf tragische Weise mit nur knapp 20 Jahren. Bei der gerichtsmedizinischen Obduktion wurde bei dem jungen Mann eine chronisch-hämolytische Anämie mit Erythrozytenindizes am unteren Normbereich festgestellt. Eine Hb-Elektrophorese samt Molekulargenetik ergab den Befund einer Sichelzellerkrankung (SCD). Diese war dem Studenten wahrscheinlich bekannt. Da er in Deutschland aber bis dahin ärztlich noch nicht untersucht worden war, gab es in keiner Datenbank einen Hinweis auf das Risiko einer Sichelzellkrise. Eine frühe und intensive Behandlung wie Bluttransfusionen, Sauerstoff - oder Stammzelltherapie hätte die Schwere des Verlaufs vielleicht verhindern können.
Auch in Großbritannien kam es 2019 im Zusammenhang mit einer Sichelzellerkrankung zu einem tragischen Vorfall mit Todesfolge. Der Fall Evan Nathan Smith erregte weltweit mit einem Gerichtsverfahren Aufmerksamkeit: Laut Berichten hatte der 21-Jährige während eines Krankenhausaufenthalts wegen Sepsis nach der Entfernung eines Gallenstents den Londoner Ambulance Service alarmiert, weil ihm in der Klinik der für ihn dringend benötigte Sauerstoff nicht zeitnah verabreicht wurde. Obwohl der Patient selbst von seiner Erkrankung wusste, war den behandelnden Ärztinnen und Ärzten diese vermutlich nicht bekannt. Erst der später am Abend hinzugerufene Hämatologe leitete eine Sauerstofftherapie ein. Leider zu spät, denn der Patient verstarb infolge multiplen Organversagens und Hirninfarkts.
Die Sichelzellerkrankung gehört zu den erblichen Hämoglobinopathien. Chronische Hämolyse, erhöhte Infektneigung und rezidivierende Gefäßverschlüsse, die zu akuten und chronischen Schädigungen aller Organe führen können, kennzeichnen diese schwere Erkrankung, die unbehandelt zum Tod führen kann. Es wird angenommen, dass beispielsweise in Deutschland mehr als 1.000 Menschen mit Sichelzellerkrankung leben – hauptsächlich Zugewanderte aus Afrika, dem Mittleren Osten, Asien, dem Mittelmeerraum sowie deren Nachkommen. Aufgrund der zunehmenden Einwanderungszahlen könnte die Anzahl der Betroffenen jedoch wesentlich höher sein.
Neben der Sichelzellerkrankung gehören auch Thalassämie und andere Hb-Anomalien zu den Hämoglobinopathien, die weltweit zu den häufigsten Erbkrankheiten zählen. Laut Fachleuten sind sie aufgrund der Zuwanderung von Menschen aus den betroffenen Regionen auch in Nordeuropa inzwischen ein unterschätztes Gesundheitsproblem. Die Diagnose und die Behandlung dieser Gruppe von Erkrankungen erfordern aufgrund der Komplexität breites Wissen und Erfahrung, die medizinisches Fachpersonal – zumindest in Deutschland – bisher leider nur schwer erwerben kann.
Unterstützung durch Mustererkennung
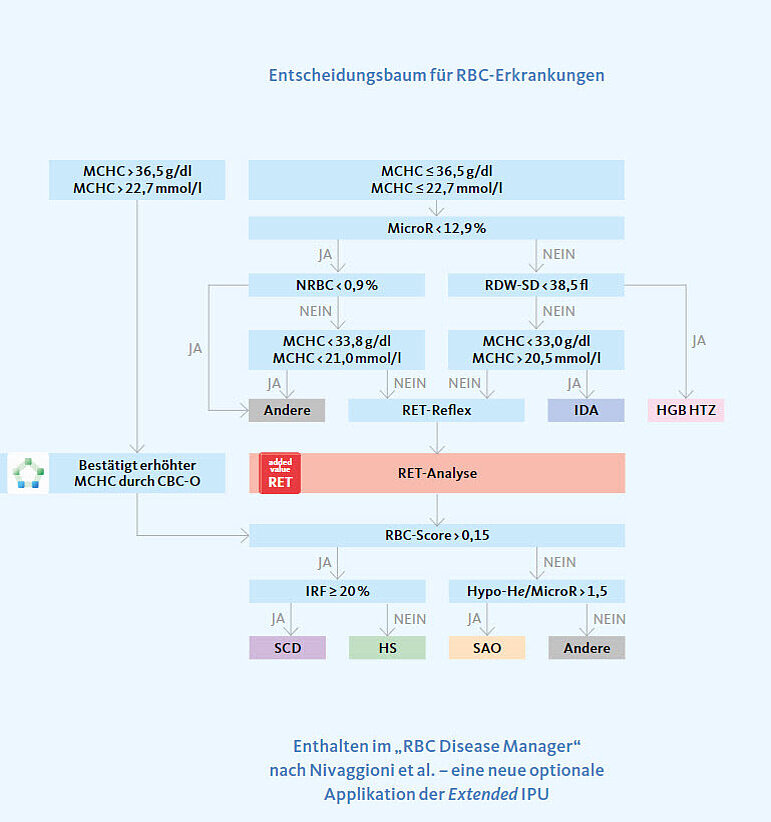
Eine gute Labordiagnostik kann dazu beitragen, Ärztinnen und Ärzten die Diagnosestellung zu erleichtern. Das Forscherteam um Nivaggioni et al. konnte einen Entscheidungsbaum zur Verfügung stellen, um bereits aus dem kleinen Blutbild spezifische Hinweise auf verschiedene RBC-Anomalitäten zu generieren. Diese Regeln nutzen in der ersten Stufe die Parameter MicroR (Anteil mikrozytärer Erythrozyten) sowie NRBC und MCHC des XN-Analysesystems. Für die zweite Stufe – etwa zur Unterscheidung zwischen Sichelzellerkrankung und hereditärer Sphärozytose – ist die Retikulozytenmessung nötig, um den von Berda Haddad et al. entwickelten „RBC-Score“ sowie den Parameter IRF (immature reticulocyte fraction) zu nutzen.
Sysmex hat diese Regeln in der Applikation „RBC Defect Workflow Optimisation (RWO)“ auf der Extended IPU zusammengefasst. Die Regeln erlauben einen differenzierten Verdacht auf Sichelzellerkrankung, hereditäre Sphärozytose, Südostasiatische Ovalozytose und hereditäre Hämoglobinopathien, wie zum Beispiel Thalassämie, sowie eine Abgrenzung zur Eisenmangelanämie.
Laboren wird es damit möglich, spezifische Hinweise auf ein mögliches Vorliegen dieser Erkrankungen zu geben – und zwar unabhängig von speziellen Kenntnissen und ohne zusätzliche Kosten oder Arbeitsaufwand. Eine weiterführende Diagnostik kann damit nicht nur gezielter, sondern wesentlich schneller eingeleitet werden. Dies kann hoffentlich dabei unterstützen, tragische Ereignisse zukünftig zu vermeiden.
Warum ist die frühe Erkennung von RBC-Erkrankungen wichtig?
Im Interview mit Dr. Saskia Brunner-Agten, Laboratoire d’analayses médicales Dr Luc Salamin, Siders, Schweiz

Frau Dr. Brunner-Agten, Sie konnten durch Ihre vorherige Tätigkeit – der Leitung der Abteilung „Erythrozyten-Funktionsdiagnostik“ am Institut für Labormedizin im Kantonsspital Aarau sehr viel Erfahrung in der Erkennung von Hämoglobinopathien sammeln. Wie schätzen Sie die Erfahrungen anderer Ärztinnen und Ärzte zu diesem Thema ein?
Hier im Wallis haben wir verhältnismäßig wenig Betroffene aus Inzidenzgebieten von RBC-Erkrankungen. Hinzu kommt, dass es Personengruppen gibt – ältere Menschen beispielsweise –, bei denen die Erkennung einer milden oder asymptomatischen Erkrankung von geringer Bedeutung ist, weil es für die aktuelle Behandlung wenig Konsequenzen hat. Durch diese Umstände haben viele Ärztinnen und Ärzte zu wenig Erfahrung aufbauen können – so ist bereits die Fragestellung auf diese Erkrankungen nicht immer präsent.
Erbliche RBC-Erkrankungen sind selten, doch wie wichtig ist ihre Erkennung?
Leiden Menschen an einer Anämie, muss die Ursache abgeklärt werden, und gerade bei einer mikrozytären Anämie sollte eben nicht nur an einen Eisenmangel gedacht werden, sondern auch an Thalassämie. Bei Thalassämie Eisen zu substituieren, kann zu einer Eisenüberladung führen, was unbedingt vermieden werden sollte, da es zu schweren Organschäden kommen könnte.
Es kann aber auch von Interesse sein, asymptomatisch Betroffene zu erkennen. Dies gilt besonders dann, wenn die Familienplanung dieser Patientinnen und Patienten noch bevorsteht. Wenn beide Elternteile asymptomatische Träger sind, kann es für das Neugeborene zu sehr schweren Erkrankungen mit dramatischen Folgen kommen. Sich dessen im Vorfeld bewusst zu sein, halte ich für wichtig. Mit sehr viel Erfahrung entwickelt sich ein Gespür dafür, hinter welchem Blutbild sich eine RBC-Erkrankung verbergen könnte, insbesondere wenn die Behandelten aus einem Inzidenzgebiet stammen könnten.
Die Gruppe um Nivaggioni et al. hat spezielle Regeln entwickelt, die Anomalitäten aus dem kleinen Blutbild erkennen und spezifische Verdachtshinweise auf Sichelzellerkrankung, Thalassämie oder sogar auf die seltene Südostasiatische Ovalozytose geben können. Was halten Sie davon?
Es ist natürlich gut, wenn automatisch mithilfe des Routineblutbilds ein spezifischer Hinweis gegeben wird. Aufgrund der eher niedrigen Inzidenz können sich nicht alle ausreichend Erfahrung aneignen, um frühzeitig eine erbliche RBC-Erkrankung zu erkennen. Es gibt so die Möglichkeit, die ärztlich Behandelnden schnell und direkt zu kontaktieren, um eine Verdachtsdiagnose mitzuteilen. Dies ermöglicht es, eine weiterführende Diagnostik zügig einzuleiten. Das ist nicht nur für die Betroffenen wichtig, sondern könnte auch Kosten einsparen. Denn eine Erkennung ist prinzipiell nicht nur für die aktuelle Behandlung im Krankenhaus von Interesse. Solche Erkrankungen begleiten Menschen ein Leben lang, sodass diese Informationen auch für künftige Behandlungen verwertet werden können. Wir nutzen beispielsweise für die Erkennung der α-Thalassämie die Huber-Herklotz-Formel, die in Aarau entwickelt wurde. Für andere RBC-Erkrankungen ist bei uns bisher noch nichts implementiert. Daher ist das auf jeden Fall interessant.
Gibt es in der Schweiz und Deutschland ähnlich wie in anderen Ländern generelle Untersuchungsprogramme oder Screenings auf genetische Erkrankungen?
In vielen südeuropäischen und asiatischen Ländern gibt es Neugeborenen-Screenings für die Erkennung von Hämoglobinopathien. In Deutschland und in der Schweiz gibt es dies bisher nicht in diesem Umfang. Aufgrund der zunehmenden Einwanderung von Menschen aus den Verbreitungsgebieten dieser Erkrankungen wird die Erkennung hereditärer Hämoglobinopathien jedoch zunehmend an Bedeutung gewinnen. Daher wären aktuell einfache Methoden von Vorteil, die auf diese seltenen Erkrankungen hinweisen könnten.
Summary
- Durch die Zuwanderung von Menschen aus den Verbreitungsgebieten von RBC-Erkrankungen ist eine frühe Erkennung inzwischen auch für medizinisches Personal in Nordeuropa wichtig, um Betroffene richtig zu behandeln sowie homozygote Geburten und Todesfälle zu vermeiden
- Sysmex hat in der Applikation „RBC Defect Workflow Optimisation (RWO)“ Regeln für die Erkennung verschiedener RBC-Erkrankungen implementiert, mit denen Labore ohne Spezialkenntnisse und zusätzliche Kosten eine entsprechende Verdachtsdiagnose erstellen können
Fotoquelle: unsplash, Marvin Zilm